줄기세포 임상연구, 잠재력과 한계 공존
알츠하이머병, 파킨슨병, 루게릭병, 헌팅턴병과 같은 신경퇴행성 질환은 전 세계적으로 환자 수가 증가하고 있지만, 아직까지 근본적인 치료법은 확립되지 않았습니다. 최근 발표된 리뷰 논문이 줄기세포 치료를 중심으로 한 임상연구 현황을 정리하고 향후 전망을 제시했습니다.
분석에 따르면 지금까지 등록된 줄기세포 임상시험은 총 94건으로, 참여자 수는 8,000명을 넘습니다. 그중 약 70%는 알츠하이머병을 대상으로 했으며, 파킨슨병, 루게릭병, 헌팅턴병 순으로 연구가 진행되었습니다. 그러나 임상 3상까지 진입한 연구는 3건에 불과해 대부분은 여전히 1·2상 단계에 머물러 있습니다.
다음 그림은 알츠하이머병(AD), 파킨슨병(PD), 루게릭병(ALS), 헌팅턴병(HD)에 대한 줄기세포 임상시험의 현황을 임상 단계별로 보여줍니다.
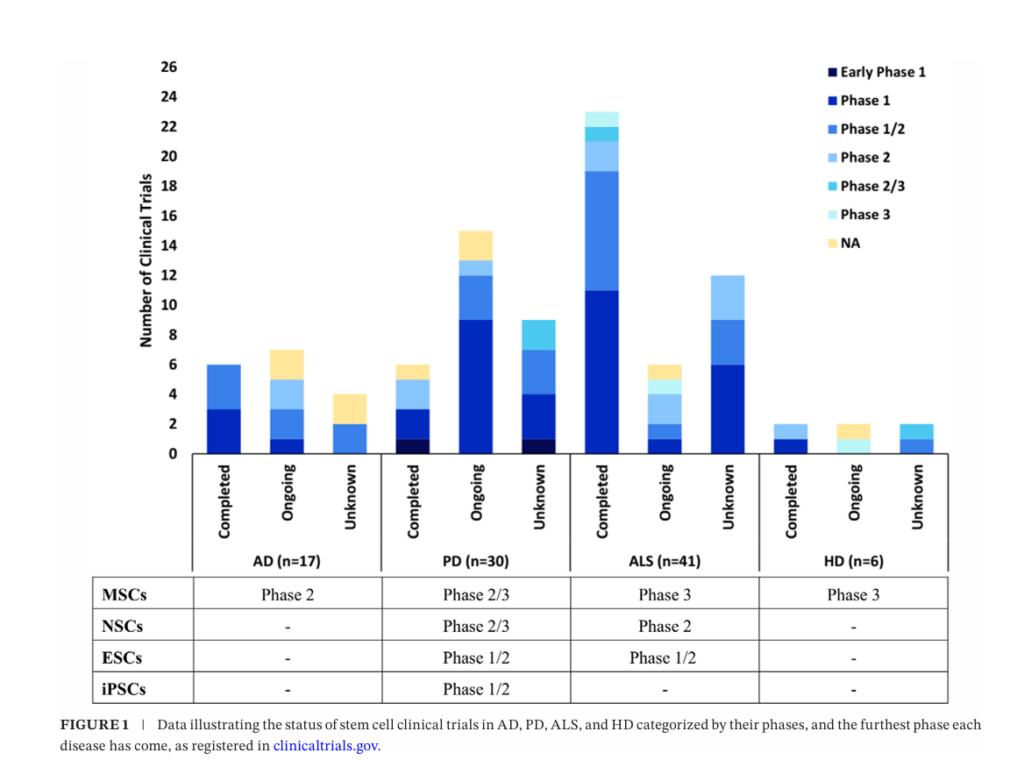
임상시험에서 가장 많이 사용된 세포는 중간엽 줄기세포(MSCs)였으며, 주로 골수, 지방조직, 제대혈에서 유래했습니다. 이 중간엽 줄기세포들은 면역조절과 신경세포 보호 효과로 주목 받고 있습니다. 신경줄기세포(NSCs)는 신경세포와 교세포로 분화 가능성이 높아 활용되었지만, 확보가 어렵고 윤리적 논란이 따릅니다. 유도만능줄기세포(iPSCs)는 파킨슨병 치료를 위해 도파민 전구세포를 만들어 이식하는 연구에 활발히 적용되고 있으며, 배아줄기세포(ESCs)는 분화 능력이 뛰어나지만 윤리적 문제로 인해 사용이 제한적입니다.
엑소좀, 새로운 치료 전략으로 부상: 혈뇌장벽 통과와 병리 단백질 억제 효과
줄기세포 연구와 더불어 최근 주목받는 분야는 엑소좀 기반 치료입니다. 엑소좀은 세포가 분비하는 미세 소포체로, 단백질과 RNA, 지질 등을 운반하며 혈뇌장벽을 통과할 수 있습니다. 생체 적합성이 높고 종양 발생 위험이 낮으며, 장기간 보관과 표준화가 비교적 용이해 임상 적용 가능성이 큽니다. 전임상 연구에서 MSC 유래 엑소좀은 알츠하이머병 모델에서 아밀로이드-β(Aβ) 축적을 완화하고 인지 기능을 개선했습니다. 파킨슨병 모델에서는 α-synuclein 응집을 억제하고 도파민 신경을 보호해 운동 기능 회복을 유도했습니다. 루게릭병 모델에서는 산화 스트레스 감소와 운동 기능 개선, 헌팅턴병 모델에서는 변형된 huntingtin 단백질 발현 억제 효과가 보고되었습니다.
임상시험 현황과 기술적 발전
엑소좀 치료 임상은 아직 초기 단계입니다. 현재 등록된 연구는 알츠하이머병 2건, 루게릭병 1건뿐이며, 파킨슨병과 헌팅턴병을 대상으로 한 임상은 아직 보고되지 않았습니다. 비록 엑소좀을 이용한 임상시험 수는 적지만, 매우 유망한 결과를 보여주고 있습니다. 예를 들어 알츠하이머병 환자를 대상으로 한 임상시험(NCT04388982)에서는 제대혈 유래 MSC 엑소좀을 비강 투여했을 때 일부 인지 기능 개선 효과가 관찰됐습니다. 특히 공학적으로 변형된 엑소좀을 이용한 연구가 활발합니다. 엑소좀 표면을 변형해 특정 수용체를 표적화하거나, 유전자·단백질·항산화제를 탑재해 뇌 전달 효율을 높이는 방식입니다. 이러한 접근법은 병리 단백질 응집 억제, 산화 스트레스 완화, 신경세포 보호 등 다양한 효과를 나타내며 치료 가능성을 확장하고 있습니다.

향후 전망: 대규모 임상과 생산 표준화 필요
연구진은 줄기세포 및 엑소좀 치료가 신경퇴행성 질환에 중요한 가능성을 열고 있다고 평가하면서도, 해결해야 할 과제로 △대규모 임상 확대 △엑소좀 생산 표준화 △장기 안전성 평가 등을 꼽았습니다. 줄기세포와 엑소좀 기반 접근법이 상호 보완적으로 발전한다면, 현재의 약물치료(예: 알츠하이머병의 Donepezil, 파킨슨병의 Levodopa 등) 한계를 보완할 새로운 치료 전략으로 자리 잡을 수 있을 것으로 전망됩니다. 이는 환자의 삶의 질 개선뿐만 아니라, 신경퇴행성 질환 연구 전반의 새로운 전환점이 될 수 있다는 평가입니다.
참고문헌:
Isik, S., Osman, S., Yeman-Kiyak, B., Shamshir, S. R. M., & Sanchez, N. M. E. (2025). Advances in neurodegenerative disease therapy: Stem cell clinical trials and promise of engineered exosomes. CNS Neuroscience & Therapeutics, 31(9), e70577. https://doi.org/10.1111/cns.70577
